课题3 制取氧气(第1课时)(教学设计)
一、教学目标
(一)知识与技能
1.了解过氧化氢制取氧气的原理
2.认识催化剂和催化作用
(一) 过程与方法
通过探究“分解过氧化氢制取氧气的反应中二氧化锰的作用”体验探究过程,初步了解探究式学习,从而形成实验探究的一般思路,学习综合分析实验现象并从中归纳结论的思维方法。
(三)情感态度与价值观
通过体验实验过程,尝试实验成功的快乐,激发学习兴趣,获得自主、合作、探究的学习态度。
二、教学重点
1.实验室用过氧化氢制取氧气的原理
2.催化剂和催化作用
三、教学难点:探究“分解过氧化氢制取氧气的反应中二氧化锰的作用”
四、教学方法 : 实验----探究式教学法、引导、分析----归纳法
五、教学过程:
【复习引入】氧气有哪些用途?如此重要的气体如何获得?引出实验室制取氧气的方法。
【新课学习】 探究用过氧化氢制取氧气
【活动1】(实验探究解疑)
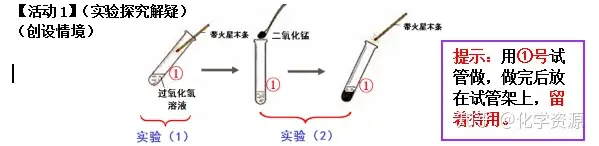
(创设情境)
(提出问题)氧气是由哪种物质产生的?
(做出猜想)1. 水 2、 二氧化锰 3. 过氧化氢 4.……
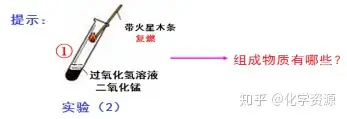
(设计实验)

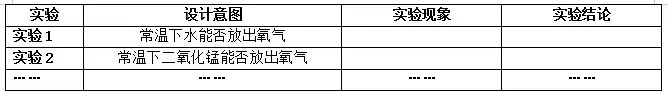
(学生进行实验)……
*由于学生的认知水平有限,学生只能提出简单的猜想1.2.3,并设计实验加以验证。老师要引导学生进一步的猜想和设计实验并完成实验。
(再质疑)会不会是二氧化锰与过氧化氢发生反应产生了氧气呢?
(实验)
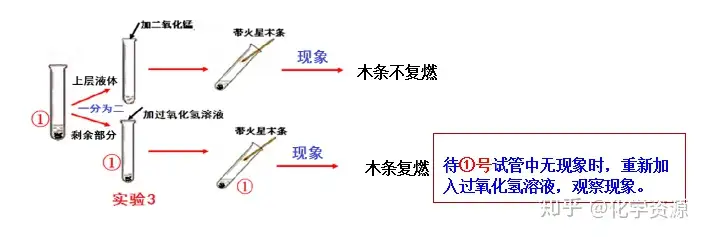
(得出结论)氧气是由 过氧化氢 产生的。
【活动2】(再探揭密)
(思考)二氧化锰在过氧化氢制氧气反应中的作用是什么呢?
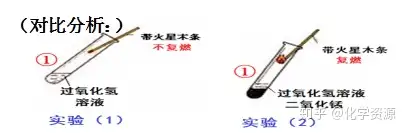
结论:二氧化锰可以 过氧化氢放出氧气的速率。
(观看视频)神奇的二氧化锰
归纳:二氧化锰在反应前后 和 没有改变。
【活动3】(构建新知)
催化剂 。
催化作用 。
分解过氧化氢制氧气的反应文字表达式 。
【活动4】(知识拓展)
1. 过氧化氢分解制氧气,除了用二氧化锰做催化剂,还有其它试剂可替代二氧化锰吗?(有条件的同学可上网查找)
2. 阅读课本40页,了解催化剂的作用。
【活动5】交流本节课的收获
【基础练习】
1.用双氧水制取氧气时,若忘记加二氧化锰,其结果是 ( )
A. 不放出氧气 B. 放出氧气速率慢 C. 放出氧气总量会减少 D. 放出的氧气不纯
2.下列有关说法正确的是( )
A、在过氧化氢溶液中加入二氧化锰可以产生更多的氧气
B、在过氧化氢溶液中加入二氧化锰可以在常温下迅速产生氧气
C、只有二氧化锰才能作过氧化氢分解的催化剂
D、催化剂在化学反应中质量和化学性质都没有发生改变
【能力提高练习】
3.“分解过氧化氢制氧气的反应中二氧化锰的催化作用”,以及“寻找新的催化剂”研究性实验,引起了化学探究小组的兴趣。
【实验探究】

【实验结论】(1)A中产生的气体是 ;
(2)实验Ⅱ、Ⅲ证明:氧化铁的 和 在反应前后均没有发生变化,可以作过氧化氢分解的催化剂;
(3)写出氧化铁催化过氧化氢分解的文字表达式 。
【实验评价】(1)设计实验Ⅳ的目的是 。
(2)若实验Ⅳ观察到D试管中产生气泡的速率更快,由此你可以得到的结论是 。
【实验拓展】查阅资料得知:氧化铜、硫酸铜、猪肝、马铃薯等也可以作过氧化氢分解的催化剂。下列有关催化剂的说法中正确的是 。
A.二氧化锰只能作过氧化氢分解的催化剂
B.同一个化学反应可以有多种催化剂
C.催化剂只能加快化学反应的速率
D.用作催化剂的物质不可能是其他化学反应的反应物或生成物
4.在二氧化锰的催化作用下,过氧化氢迅速分解生成氧气和水。哪些因素还影响着过氧化氢分解的速率?课外活动小组同学进行了更深入的探究:
探究实验一:浓度对过氧化氢分解速率的影响

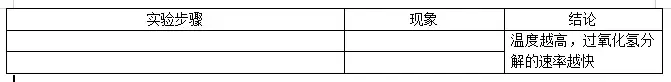
请你设计:(实验用品:试管、烧杯、热水、冷水、5%的过氧化氢溶液、15%的过氧化氢溶液)
探究实验二:温度对过氧化氢分解速率的影响