4.4 如何书写化学方程式
【学习目标】:
1、知识与技能:
(1)进一步理解化学方程式的涵义
(2)正确书写简单的化学方程式
(3)了解书写化学方程式应遵循的两个原则
2、过程与方法:
(1)在练习书写方程式的过程中重点掌握化学方程式的配平方法。
(2)归纳正确书写化学方程式的步骤。
(3)初步学会用化学方程式来表示所获得的信息。
3、情感、态度与价值观:
在学习过程中意识到任何事都必须尊重客观事实,在学习中体会学习的乐趣,体会化学用语的方便和实用。
【学习重难点】
1、重点:化学方程式的书写原则
2、难点:化学方程式的配平方法
【课时安排】
第一课时:正确书写化学方程式
第二课时:学会利用化学方程式的简单计算,正确掌握计算的格式和步骤。
第一课时
【教学过程】
[复习引入]写出下列化学反应的文字表达式。
1.木炭燃烧_____________________________________________
2.用氯酸钾制氧气_______________________________________
怎样把文字表达式写成化学方程式呢?
一、什么是化学方程式
一个化学方程式能提供给我们哪些信息?
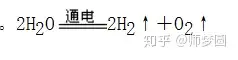
化学方程式提供的信息包括(化学方程式的意义):
1.质的方面:表明反应物和生成物的种类及反应条件。
(上例中反应物为C和O2,生成物为CO2,反应条件为加热);
2.量的方面:表明参加化学反应的各物质的质量比(12∶32∶44=3∶8∶11)符合质量守恒定律。
仅仅写出反应物、生成物以及反应条件并不能表示一个化学方程式,这仅仅完成了书写化学方程式的第一步。那么如何才能正确地书写化学方程式呢?
二、怎样书写化学方程式
(一)书写原则
化学方程式是用来表示化学反应的,既然化学反应的发生不是凭空想象,因此,在书写化学方程式时必须遵守两个原则。
1、是必须以客观事实为基础,绝不能凭空臆想、臆造事实上不存在的物质和化学反应。
2、是要遵守质量守恒定律,等号两边各原子的种类与数目必须相等。
(二)书写步骤
我们现在再以电解水生成氢气和氧气这个反应为例来归纳书写化学方程式的步骤。
1.“写”根据实验事实在短线左边写出反应物的化学式,右边写出生成物的化学式,不只一种物质的用“+”连接。 H2O——H2+O2
2.“配”在式子两边的化学式前配上适当的化学计量数,使短线左右两边达到原子的种类相同,数目相等,符合质量守恒定律。(目的使式子两边各原子的种类和个数就相等) 2H2O——2H2+O2
[说明]切记决不能改变化学式右下角的数字,所配化学式前边的化学计量数应是最简整数比。
3.“注、标”注明反应发生的条件;标上箭头。
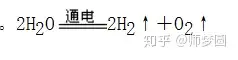
(1)通电就是该反应的条件。
(2)如果反应物中没有气体,而生成物中出现了气体,需在气体物质的化学式右边注“↑”在溶液中的反应,反应物中没有固体,而生成物中出现了固体,则需在固体物质化学式右边注“↓”符号。
4.“等”将短线变为等号,意味着遵守质量守恒定律。
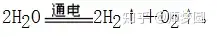
[补充说明]
①“加热”是最常用的化学反应条件,“加热”用符号“△”表示。
②若反应进行只需1个条件,就把此条件写在短线上方,若需2个或多个条件,则分开写在短线上、下两方。
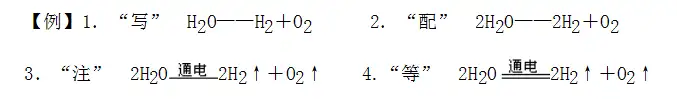
[课堂练习]配平下列化学方程式并注明条件。
1.Al+O2——Al2O3 2.H2O2——H2O+O2 3.Mg+O2——MgO
三、化学方程式的读法
1.“+”不能读“加”,应读“和”与”“跟”;
2.“==”不能读“等于”,应读“生成”;
3.化学式应读成物质的名称;
4.反应条件也应读出。
[小结]
1、知道了书写化学方程式的原则和步骤,及书写化学方程式应该注意的事项。
2、知道化学方程式的意义及读法。
[课外练习]习题1、2、3、

